정책/뉴스
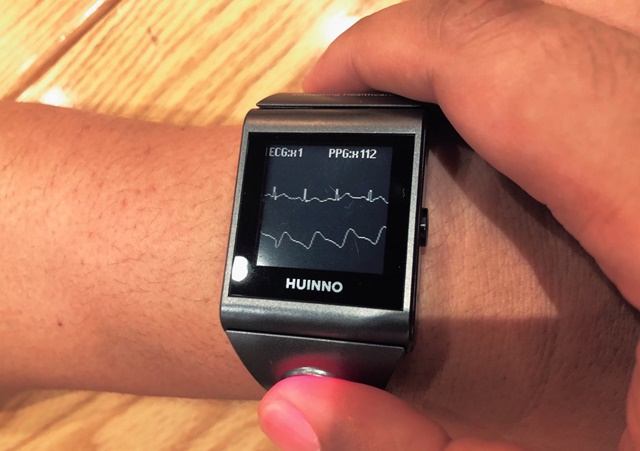 ▶휴이노·고려대 안암병원의 손목시계형 심전도 장치│휴이노
▶휴이노·고려대 안암병원의 손목시계형 심전도 장치│휴이노
정보통신기술(ICT) 분야 규제 샌드박스 1호 제품인 손목시계형 심전도 측정기가 국내 최초로 의료기기 승인 허가를 받았다. 벤처기업 휴이노는 3월 25일 심전도 측정기인 ‘메모워치’가 식품의약품안전처에서 2등급 의료기기 승인 허가를 받았다고 밝혔다.
이번 허가로 심장질환을 앓는 환자는 상당한 편의를 제공받을 수 있게 됐다. 손목시계형 장치에서 얻은 심전도 데이터를 의사에게 전송해 이상 징후가 있을 때는 내원 안내를 받아 검사할 수 있기 때문이다. 또 의사의 원격 모니터링으로 내원이 필요하지 않은 환자는 번거로움을 줄일 수 있다.
이에 따라 국내 의료전달체계에도 긍정적인 변화를 줄 것으로 기대된다. 심장박동에 이상을 느끼면 지금은 가벼운 증세라도 대형 병원으로 가는 경우가 많다. 메모워치를 활용하면 가벼운 증상의 환자는 1·2차 의료기관으로 안내받는다. 동네 의원이나 지역 병원으로 환자를 보내 대학병원에 환자가 몰리는 현상을 줄일 수 있는 것이다. 중증의 환자는 증상이 호전되면 1·2차 의료기관으로 옮기도록 안내한다. 이렇게 되면 환자들은 가까운 병원에서 긴 대기 시간 없이 빠른 진료를 받을 수 있다. 의사 입장에서도 지속적으로 측정된 환자의 심전도 정보를 모니터링하고 대면 진료에 활용할 수 있어 환자 관리의 효율성이 높아진다. 길영준 휴이노 대표는 “식약처의 의료기기 인증에는 1300가지 공통규격과 100여 가지 개별규격 검사 항목이 있다. 이 검사들을 통과해 안전성을 인증받아 제품을 출시하게 됐다”고 말했다.
올해 상반기 제품 출시해 시범 서비스
이번에 허가를 받은 휴이노는 문재인 대통령이 2월 12일 국무회의에서 ‘규제 탓에 외국보다 시판이 늦어진 사례’로 거론했던 업체다. 휴이노는 같은 기능이 탑재된 애플의 ‘애플워치 4’가 나오기 3년 전인 2015년에 스마트워치를 개발했지만, 법규의 불명확성으로 허가를 받지 못해 선수를 빼앗겼다. 그러나 과학기술정보통신부가 2월 14일 휴이노가 개발한 손목시계형 심전도 측정기를 활용한 심장관리 서비스를 ICT 분야 규제 샌드박스 1호 제품으로 선정하고 ‘실증 특례’를 부여하면서 제품 출시의 길이 열렸다.
식약처의 인증을 받음에 따라 휴이노는 올해 상반기 중에 제품을 출시해 시범 서비스를 실시할 계획이다. 실증 사업에 참여할 환자는 휴이노와 고려대 안암병원이 함께 모집한다. 길 대표는 “우리 회사와 고려대 병원 누리집 등으로 신청 접수를 받아, 고시한 4~5개 질병군의 증상이 있는 환자 중 선별할 예정”이라고 밝혔다. 일반인들도 이 서비스가 인증을 얻으면 대면 진료에 활용할 수 있을 것으로 예상된다. 휴이노의 스마트워치 가격은 기록·분석용 앱을 포함해 35만 원 선이다. 길 대표는 “환자뿐 아니라 건강에 관심이 많은 사람들도 이 서비스를 이용할 수 있도록 기술을 개발하겠다”고 말했다.
한광덕 기자
K-공감누리집의 콘텐츠 자료는 「공공누리 제4유형 : 출처표시 + 상업적 이용금지 + 변경금지」의 조건에 따라 자유롭게 이용이 가능합니다. 다만, 사진의 경우 제3자에게 저작권이 있으므로 사용할 수 없습니다. 콘텐츠 이용 시에는 출처를 반드시 표기해야 하며, 위반 시 저작권법 제37조 및 제138조에 따라 처벌될 수 있습니다.
[출처] K-공감누리집(gonggam.korea.kr)





















